6月6日,美国临床肿瘤学会(ASCO)公布了首个针对HER2低表达晚期乳腺癌的III期临床研究DESTINY-Breast04研究结果。会上,Memorial Sloan Kettering Cancer Center的Shanu Modi博士以“Our history is not our destiny——我们的历史不是命运。”为题汇报了DESTINY-Breast04最新数据,会议现场经久不息的掌声里是专家们对于见证HER2低表达这一乳腺治疗新领域诞生的激动与振奋。
作为乳腺癌领域唯一入选全体大会环节的重磅研究,DESTINY-Breast04将为乳腺癌的临床实践带来哪些颠覆性变革呢?历史不是命运,那它又将如何改写呢?
抗 HER2 药物靶向
HER2低表达乳腺癌漫漫前路
抗HER2治疗前时代,HER2阳性乳腺癌由于其侵袭性强、预后差、复发风险高等特点,一度被称为“粉红丝带上的黑蝴蝶”,抗HER2药物的诞生彻底改变了 HER2 阳性乳腺癌患者的治疗结局。那HER2低表达的患者是否也能从抗HER2的药物中获益呢?人们也开始对此进行探索。
事实上DESTINY-Breast04研究的主要对象——T-DXd,也称 DS-8201a并非第一个在HER2低表达领域进行探索的抗HER2药物。抗HER2 单克隆抗体(曲妥珠单抗和帕妥珠单抗)、抗 HER2 疫苗(nelipepimut-S)和首个抗 HER2 ADC药物TDM1在前二十年尝试中从未获得理想的成果。
NSABP B-47 是一项大型随机 3 期试验,该试验招募了 3270 名 HER2低表达患者接受曲妥珠单抗联合化疗与单独化疗相比,未能证明曲妥珠单抗有显著获益。

无独有偶, 另一个抗HER2的单抗药物帕妥珠单抗,在一项 II 期试验中,单独使用帕妥珠单抗用于既往治疗过的 HER2 阴性或低表达患者,也没有收获理想的结果。
T-DM1作为乳腺癌领域第一个ADC药物,由靶向 HER2 的载体曲妥珠单抗通过不可切割的硫醚接头与强效抗微管蛋白美登素衍生物 DM1 结合组成。但与前两者不同,T-DM1 从未在 HER2低表达乳腺癌中进行前瞻性研究。尽管如此,在两项 II期试验中,在既往接受曲妥珠单抗治疗的 HER2 阳性转移性 乳腺癌患者中探索了 T-DM1 的疗效和安全性,根据 HER2 状态的中心实验室评估进行的探索性分析发现,与 HER2 阳性乳腺癌患者相比,HER2低表达的乳腺癌患者中 T-DM1 的临床活性较差。

所以既往抗HER2治疗药物的相关临床研究结果表明,抗HER2治疗药物只对免疫组化HER2 3+或HER 2+且FISH 阳性的患者有显著获益。
HER2低表达晚期乳腺癌
未愈之痛
由于抗HER2药物在HER2低表达领域多次探索均以失败告终,因此,在过往的临床诊疗中只有HER2阳性与阴性之分,HER2阴性患者(IHC0,IHC1+,IHC2+/ISH-)主要根据患者激素受体表达情况,选择不同的治疗路径。
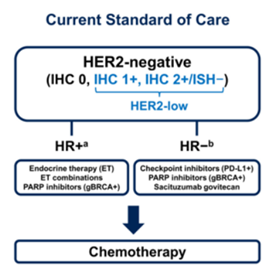
但HER2低表达的患者被认为缺少特异性可作用的靶点,在治疗进展后的靶向治疗选择较为有限,最常接受单药姑息性化疗。而Destiny-Breast04可能为多达50%的乳腺癌患者提供新的治疗标准从而改善其生存预后。
DB04结果首次显示抗HER2疗法能够使HER2低表达患者获益

DESTINY-Breast04 研究是一项全球 208 个中心的 III 期随机对照研究。研究计划入组 540 例 HER2 低表达(IHC 2+且 ISH− 或 IHC 1+)、既往接受过 1 或 2 线化疗的不可切除或转移性乳腺癌患者,按照 2:1 比例随机分配至 T-DXd 组(5.4 mg/kg,IV,q3w)或研究者选择方案组(卡培他滨、艾立布林、吉西他滨、紫杉醇或白紫);主要终点是独立盲法中心(BICR)评估 HR 阳性、HER2 低表达患者的 PFS(无进展生存期)。关键次要终点(在主要终点之后进行分层测试)包括 BICR 在完整分析集中(HR+/−) HR+ mBC 患者的无进展生存期(PFS)和总生存(OS)。其他终点为客观缓解率、缓解持续时间、安全性,以及对 HR−mBC 患者的探索性分析。

(DESTINY-Breast04 研究设计;图源 ASCO)
截至 2022 年 1 月 11 日,557 名接受随机分组的患者中,494 名(88.7%)为 HR 阳性,63 名(11.3%)患有 HR 阴;373 和 184 名患者(88.7% 和 88.6% HR+ mBC)分别分配给 T-DXd 和 TPC。中位随访时间为 18.4 个月(95%CI:17.9-19.1)。T-DXd 的中位治疗时间为 8.2 个月(范围:0.2-33.3),TPC 为 3.5 个月(范围 0.3-17.6)。
在 HR 阳性队列中,T-DXd 组的中位 PFS 为 10.1 个月,医生选择组为 5.4 个月(疾病进展或死亡的 HR = 0.51;P<0.001),OS分别为 23.9 个月和 17.5 个月(死亡的 HR = 0.64;P = 0.003)。在所有患者中,中位 PFS T-DXd 组为 9.9 个月医生选择组为 5.1 个月(疾病进展或死亡的 HR = 0.50;P<0.001),OS分别为 23.4 个月和 16.8 个月(死亡 HR = 0.64;P = 0.001)。
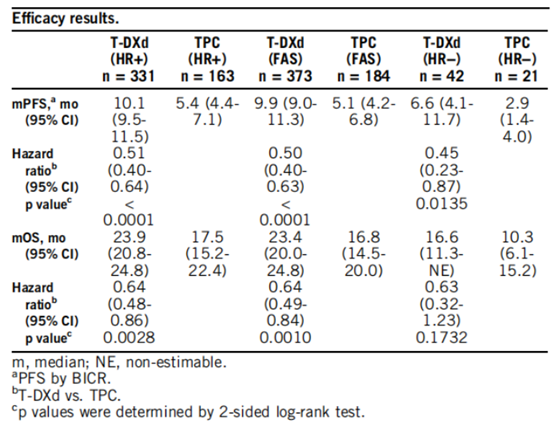
最终研究结果显示,DESTINY-Breast04 研究达到了主要终点,即 T-DXd 相较于研究者选择方案,可显著降低 HR 阳性、HER2 低表达患者的疾病进展或死亡风险。而且关键次要终点也有获益,包括无论 HR 状态(阳性或阴性)、HER2 低表达患者的 PFS,以及 HR 阳性、HER2 低表达患者和无论 HR 状态(阳性或阴性)患者的 OS 均有改善。
总结
DESTINY-Breast04 研究是第一个针对 HER2 低表达患者并获得阳性结果的III期试验,为 HER2 低表达患者的精准治疗提供了新的高质量循证医学证据,使得HER2低表达成为一种新亚型。
正如Shanu Modi教授在ASCO新闻发布会上所说:“DESTINY-Breast04的研究证实HER2低表达转移性乳腺癌是可以靶向治疗的患者群体,T-DXd是此类患者的新治疗标准”。ASCO会议讨论专家、埃默里大学Winship癌症中心Jane Lowe Meisel教授指出:“这项研究结果毫无疑问将改变我们的临床实践,该药物将使传统上治疗十分困难的全新患者群体获益。该项试验将从根本上改变我们对HER2状态的认知以及对转移性乳腺癌的分类。”
