6月22日,第一三共宣布已向欧洲药品管理局 (EMA) 提交trastuzumab deruxtecan(DS-8201,T-Dxd)单药治疗既往曾接受全身治疗或在完成辅助化疗期间或6个月内出现复发的不可切除或转移性HER2低表达(IHC1+或IHC2+/ISH-)乳腺癌患者的上市申请,该申请已得到EMA确认并由EMA的人类使用药品委员会(CHMP)开始科学审查程序。

这一申请是基于在2022年ASCO年会上公布并同时发表在《新英格兰医学杂志》上的DESTINY-Breast04 III期临床试验(NCT03734029)的研究结果。

DB04 改写HER2低表达患者的命运
DESTINY-Breast04共入组HER2低表达晚期乳腺癌化疗失败患者557例,按2∶1的比例随机分为两组:DS-8201(5.4 mg/kg)组373例、医生选择化疗(TPC,卡培他滨、艾日布林、吉西他滨、紫杉醇或白蛋白紫杉醇)组184例,其中HR+494例(88.7%,DS-8201组331例、TPC组163例)、HR-63例(11.3%)。
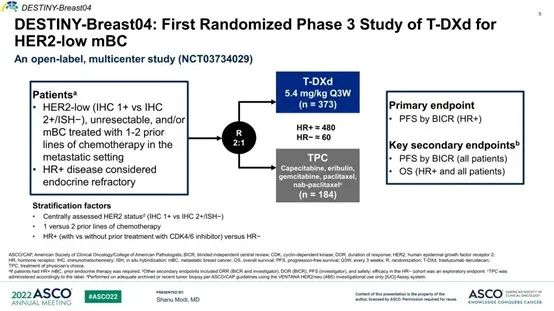
主要终点为HR+患者的无进展生存(PFS)。关键次要终点为全部患者(FAS;HR+/−)的PFS、HR+患者和全部患者的总生存(OS)。中位随访时间为18.4个月(95% CI:17.9-19.1)。
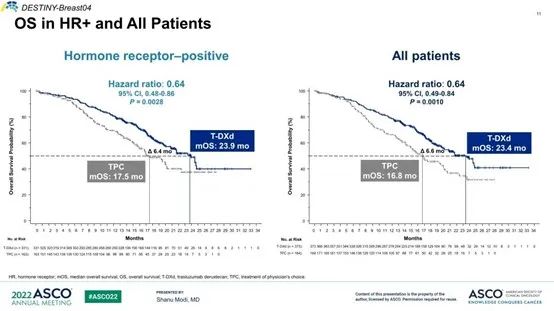
在HR+队列中,与TPC相比,DS-8201将患者疾病进展或死亡风险降低49%(HR=0.51,95% CI:0.40-0.64;P<0.001),DS-8201组和TPC组的中位PFS分别为10.1个月和5.4个月。DS-8201还将死亡风险降低了36%(HR=0.64,95% CI:0.48-0.86;P=0.003),两组的中位OS分别为23.9个月和17.5个月。
在全体患者中,与TPC相比,DS-8201将患者疾病进展或死亡风险降低50%(HR=0.50,95% CI:0.40-0.63;P<0.001),DS-8201组和TPC组的中位PFS分别为9.9个月和5.1个月。DS-8201还将死亡风险降低了36%(HR=0.64,95% CI:0.49-0.84;P=0.001),两组的中位OS分别为23.4个月和16.8个月。

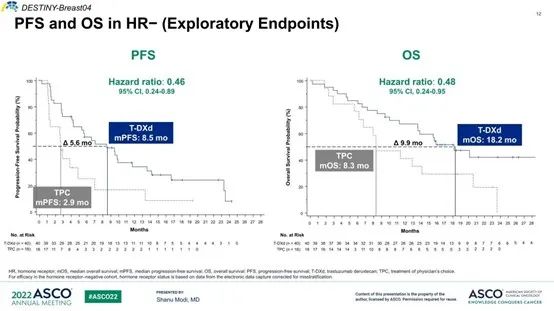
在HR-队列中,与TPC相比,DS-8201将患者疾病进展或死亡风险降低54%(HR=0.46,95% CI:0.24-0.89),两组中位PFS分别为8.5个月和1.9个月;DS-8201组较TPC组死亡风险降低了52%(HR=0.48,95% CI:0.24-0.95),两组中位OS分别为18.2个月和8.3个月。值得一提的是,这一患者群体传统上被定义为三阴性乳腺癌。
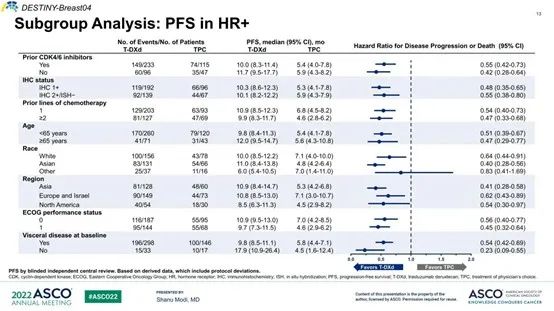
对不同患者亚群的探索性分析显示,无论患者是否曾经接受过CDK4/6抑制剂的治疗,或此前接受过化疗种类的多少,DS-8201都显示出一致的疗效。
综上,DESTINY-Breast04结果显示,与标准治疗相比,无论HR状态如何,患者的PFS和OS均有统计学显著和临床意义显著的获益,且总体安全可控。
DESTINY-Breast04是第一个针对HER2低表达患者并获得阳性结果的III期临床试验,这一里程碑式的突破意味着DS8201或将为约一半乳腺癌患者带来全新治疗模式!
总 结
在2020年的全球癌症统计中,乳腺癌超过肺癌,成为全球最常见的癌症类型。以往,根据肿瘤细胞的HER2蛋白表达量,乳腺癌患者主要以阴阳区分,即HER2阳性”和“HER2阴性,其中阳性患者大约占了约20%,阴性占了约80%。而HER2低表达乳腺癌目前仍被视为HER2阴性,占乳腺癌患者的比例超过50%。然而这些患者在治疗进展后选择有限,此前靶向HER2的单克隆抗体疗法在这一群体中也未显示出显著疗效。

DESTINY-Breast04数据将庞大的HER2低表达乳腺癌患者确定为目标人群,成为这部分患者的新治疗标准。新诊疗标准落实后,DS-8201将开辟的一个2.5倍于“HER2阳性”的市场空间。这些数据也将迫使科研人员和临床医生重新思考和定义乳腺癌HER2-类别中的亚组,而这些改变都源于DS-8201的横空出世。
DS-8201目前已在香港正式获批,如有需要对接香港医疗机构的患者及其家属可以联系找药宝典客服进行对接(vx:zhaoyaobaodian007)。期待DS-8201也早日在中国大陆获批,惠及更多患者!
