近日,J Natl Compr Canc Netw杂志(IF=7.57)发表了篇三阴乳腺癌的综述,详细介绍了免疫检查点抑制剂(ICIs)单药以及联合化疗、靶向和新型免疫疗法的联合策略,展现了三阴乳腺癌免疫抑制剂治疗的一个框架,方便大家理解免疫抑制剂在三阴乳腺癌的现有临床经验和正在进行的研究现状。下面我们来一起看看:

三阴性乳腺癌(TNBC)是雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体(HER2)表达均为阴性的乳腺癌亚型,占所有乳腺癌的15%~20%。多年来化疗一直是标准治疗,患者有中位OS只有12到18个月,且容易耐药复发,预后较差,因此迫切需要改进疗法。以PD-1/PD-L1免疫检查点抑制剂为代表的免疫治疗近年在许多瘤种中都取得了重大进展,在TNBC领域也有突破。
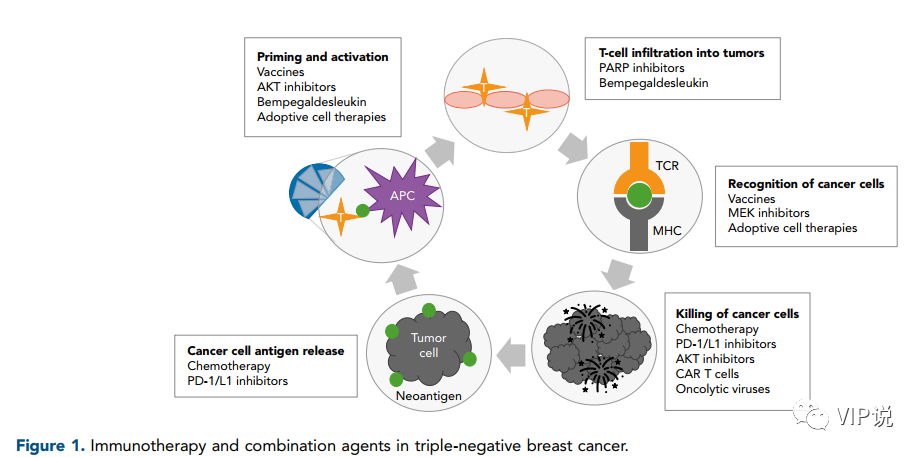
三阴乳腺癌的一些特征会使得它对PD-1/PD-1抑制剂治疗更加敏感:
TNBC有更多的肿瘤浸润淋巴细胞(TILs),在TNBC早期高TILs往往和更好的预后相关。
无论是肿瘤细胞还是免疫细胞上,TNBC中都有着相对较高的PD-L1表达。
TNBC具有大量的非同义突变,ICIs可以强化肿瘤特异性新抗原对特异性T细胞的激活,发挥抗肿瘤效应。
因此免疫治疗在三阴乳腺癌中是大有可为的
1 晚期TNBC免疫治疗
1 免疫单药治疗
ICIs单药治疗有效率低,ORR范围从未筛选人群的5%到一线PD-L1阳性人群的23%不等。
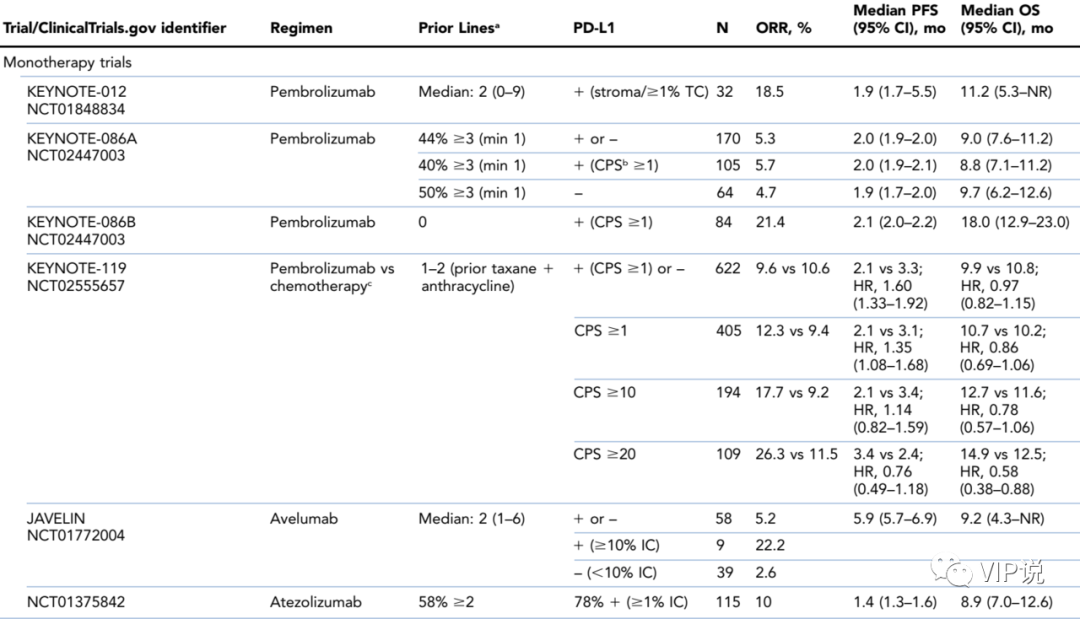
早期Ⅰb期的KEYNOTE-012研究在32例PD-L1阳性的患者中帕博利珠单抗显现出令人鼓舞的单药治疗效果,ORR达到18.5%。
在II期KEYNOTE-086研究中,采用帕博利珠单抗治疗PD-L1阳性的晚期TNBC,一线治疗有效率为21.4%,二线及以后的有效率仅为5.7%,提示早期使用免疫治疗疗效较佳,但并不优于传统化疗。
Ⅲ期KEYNOTE-119研究入组的2-3线的mTNBC,与化疗相比帕博利珠单抗单药在ORR、PFS、OS上都没有显著改善,尽管CPS≥10患者有生存获益趋势。
Ⅰb期的JAVELIN研究在58例mTNBC中Avelumab治疗的ORR为5.2%。
阿特朱单抗在早期Ⅰ期研究纳入的115例后线患者中ORR为10%。
这些都提示免疫抑制剂单药治疗获益有限,暂时不推荐单药使用。未来研究的方向应集中于免疫治疗联合化疗/靶向治疗/放疗及其他的联合治疗策略上。
2 免疫联合治疗
在TNBC患者中ICIs联合化疗比单药使用疗效更好些。
ENHANCE-1研究为帕博利珠单抗联合艾日布林化疗在既往0-2线治疗过的HER2阴性乳腺癌中的研究,在入组的106例患者中ORR达26.4%。
同样的Atezolizumab联合白蛋白紫杉醇在既往0-2线治疗过的小样本研究中,33例患者ORR高达39.4%,基于该组合良好的疗效,且免疫治疗可能早用效果更好,公司后续开展了在一线TNBC中的大型IMpassion130的III期研究。
结果显示, Atezolizumab联合白蛋白紫杉醇一线治疗mTNBC患者能够改善ITT人群和PD-L1阳性患者的PFS以及PD-L1阳性(SP142检测)患者的OS(HR=0.71),使得PD-L1阳性mTNBC的中位总生存可高达25个月,远高于化疗的12-18个月。基于此项研究结果,2019年3月8号,Atezolizumab被美国FDA批准联合白蛋白紫杉醇用于PD-L1阳性的不可手术的局部晚期/转移性三阴性乳腺癌的一线治疗,也算是作为妇女节的贺礼。

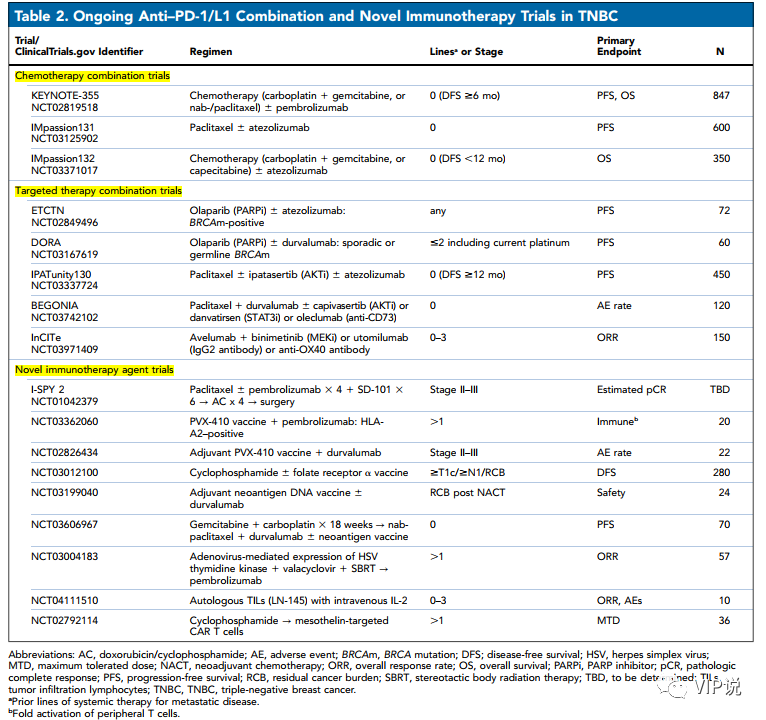
2 晚期TNBC中正在开展的重点临床研究
正在进行中的一线TNBC重点研究包括IMpassion131、IMpassion132以及KEYNOTE-355研究等。KEYNOTE-355是一项评估帕博利珠单抗联合化疗(白蛋白紫杉醇、紫杉醇或吉西他滨/卡铂) 对比化疗用于一线治疗既往未经治疗的局部复发性不可手术或转移性TNBC的随机、双盲、Ⅲ期研究。主要终点是PFS和OS(在所有患者CPS≥1及CPS≥10的PD-L1阳性患者),近期该研究公布在CPS ≥10的PD-L1阳性mTNBC患者中达到了PFS的主要终点。
可以看到未来的方向是免疫抑制剂联合化疗/靶向/新型免疫疗法,例如BRCA/PI3K/ AKT/mTOR/ MEK/ CDK4/6抑制剂、雄激素受体抑制剂、ADC药物、肿瘤疫苗、溶瘤病毒和过继免疫疗法(TIL、CAR-T)等等。部分相关方向研究将在后文进行详细介绍。
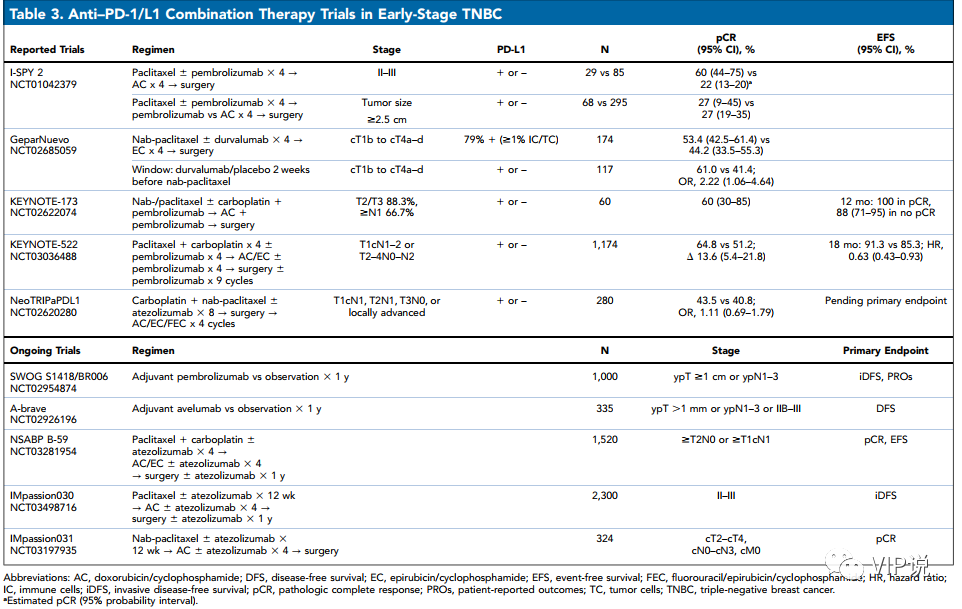
3 早期TNBC免疫新辅助/辅助治疗
ICIs联合化疗在早期TNBC中K药取得了成功,而I药和T药是暂时失败的。
I期KEYNOTE-173研究显示帕博利珠单抗,pCR率可达60%。
Ⅱ期I-SPY2研究中联合帕博利珠单抗,pCR率能够提高38%(60% vs 22%),可能与蒽环类药物免疫刺激作用有关,增加肿瘤内免疫效应和抗原摄取和提呈。基于以上两项研究,FDA授予帕博利珠+化疗在高危早期TNBC患者新辅助治疗的突破性药物资格。
Ⅱ期GeparNeuvo研究显示联合durvalumab,ITT人群的pCR率未显著提高(53.4% vs 44.2%)。
III期NeoTRIPaPDL1研究结果显示,在白蛋白紫杉醇+卡铂基础上联合atezolizumab单抗新辅助治疗并未显著提高pCR率(43.5% vs 40.8%),但多因素分析提示PD-L1+表达对提高pCR率的影响最显著(OR 2.08),主要终点EFS和其他疗效终点还在继续随访。
III期KEYNOTE-522研究在早期TNBC含铂新辅助化疗方案中加入帕博利珠单抗,pCR提高了13.6%(64.8% vs 51.2%),具有统计学和临床意义,同时帕博利珠单抗新辅助+辅助治疗能延长患者18个月EFS(91.3% vs 85.3%)。但这个研究中淋巴结阴性的患者中获益较少,说明这个方案可能对早期淋巴结阴性和高TIL患者的风险是胜过收益,这些患者用现有标准治疗就可以获得不错的生存获益。目前FDA还没有批准该方案用于新辅助治疗,仍需等待EFS随访结果。
相似的研究设计,不同的研究结果,提示免疫治疗在TNBC新辅助治疗的应用还需要进一步探索和长期生存随访结果支持。同时众多早期TNBC的围手术期(NSABP B-59、IMpassion 30)、术前新辅助(IMpassion 31)及术后辅助免疫治疗研究(A-Brave、SWOG S1418研究)都正在探索进行中。
4 TNBC中免疫抑制剂联合靶向或其他免疫治疗
(1) PARP抑制剂联合ICIs
mTNBC中的PD-1 / L1抑制剂使用部分会出现原发耐药,一些免疫联合靶向的新组合也正在探索克服潜在耐药。TNBC目前针对≥2线的BRCA突变患者治疗批准了2种PARP抑制剂(奥拉帕利和他拉唑帕利),因此PARP抑制剂联合ICIs也是火热的研究方向。
II期TOPACIO研究是PARP抑制剂联合ICIs用于转移性或晚期TNBC的首个临床研究,入组55例TNBC患者,在尼拉帕利联合帕博利珠单抗治疗的ITT人群中ORR达21%。在15例BRCA基因突变的患者中ORR高达47%,中位PFS为8.3个月。基于交叉试验比较的限制,此ORR略低于PARP抑制剂单药在gBRCA突变人群的(奥拉帕利 55%和 他拉唑帕利62%),但是中位PFS是高于这两个PARP抑制剂单药在TNBC亚组中的数据(奥拉帕利 5.5m和他拉唑帕利 5.8m)。
另一个在TNBC中探索PARP抑制剂联合ICIs的是MEDIOLA研究,在BRCA突变的mTNBC患者中Durvalumab联合奥拉帕利的ORR为58.8%,mPFS为4.9月,和PARP单药治疗类似。
不同的PARP抑制剂、非随机的设置和小样本的探索研究限制了结论的可信度,因而一些样本量多些的研究正在进行探索,例如ETCTN研究(奥拉帕利+Atezolizumab)、DORA研究(奥拉帕利+durvalumab)以及I-SPY 2队列研究(奥拉帕利+durvalumab +化疗新辅助)。
(2)AKT抑制剂联合ICIs
AKT抑制剂在TNBC中另一个重要的研究靶点。2019年AACR会议报道的Atezolizumab联合小分子AKT抑制剂Ipatasertib和紫杉类药物在26例转移性TNBC一线患者中研究提示,联合使用ORR率高达73%,且不依赖于PD-L1的表达与否或PIK3CA/AKT的状态。目前该方案的Ⅲ期研究IPATunity130正在进行中。
另一个AKT抑制剂capivasertib联合durvalumab和紫杉醇的BEGONIA研究也正在进行中。
(3)MEK抑制剂联合ICIs
MEK抑制剂联合免疫检查点抑制剂也引起了广泛关注。临床前研究表明,MEK抑制可以上调PD-L1和MHC表达并增强PD-1 / L1抑制剂的抗肿瘤活性。II期COLET研究探索了MEK抑制剂考比替尼联合Atezolizumab和紫杉烷的三药方案在63例初治TNBC 患者中疗效和安全性,显示该三联体疗法的活性中等,在紫杉醇和白蛋白紫杉醇组的ORR分别为34.4%和29.0%,中位PFS分别为3.8和7.0个月。但是该研究一开始设计就并非旨在确定PD-1抑制剂能够增加MEK抑制剂和紫衫类组合的疗效,相应的研究InCITe研究(Avelumab +binimetinib (MEKi)组 )也正在开展中。
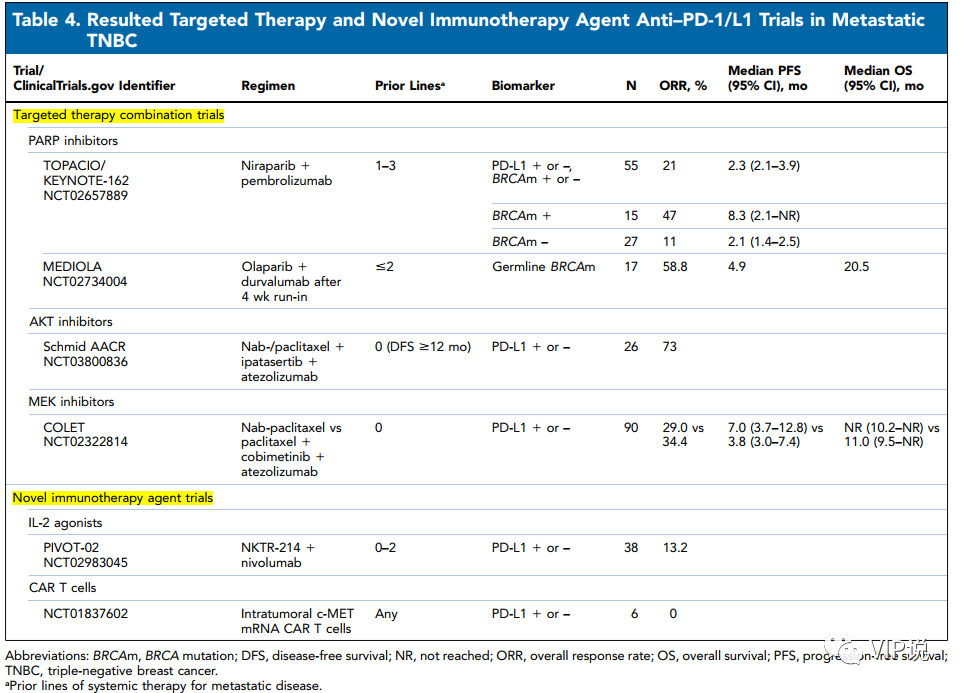
(4)免疫调节因子联合ICIs
为了克服TNBC中免疫治疗的一些缺陷,一些免疫抑制剂联合新的免疫治疗策略也正在临床开发中。其中一个策略是IL-2途径激动剂NKTR-214, I / II期PIVOT-02研究评估了38例mTNBC患者中NKTR-214联合nivolumab治疗的ORR达13.2%,具有持久性不无论PD-L1表达。另一个是肿瘤内的Toll样受体9(TLR9)激动剂SD-101,I-SPY 2研究就正在探索SD-101联合帕博利珠单抗新辅助治疗。
目前乳腺癌疫苗联合PD-1 / L1的多项试验也正在招募TNBC患者,例如PVX-410疫苗(NCT03362060,NCT02826434),叶酸受体α疫苗(NCT03012100)和新肿瘤抗原疫苗(NCT03199040,NCT03606967)。
此外,免疫抑制剂联合溶瘤病毒(NCT03004183)和过继细胞疗法(TIL转移和CART)的一些研究(NCT04111510,NCT02792114)也都在开展中。
这些新颖的免疫疗法尽管是初步的并且需要广泛的临床验证,有助于增强对乳腺癌免疫治疗的了解,发展出未来有效的免疫疗法。
