乳腺癌内分泌治疗由于具有较好的疗效,能显著降低复发风险等优势,在临床中贯穿着乳腺癌患者(激素受体阳性患者)从早期的新辅助治疗到术后辅助及复发解救的全部治疗过程。
同时,随着内分泌药物的不断更新迭代,治疗手段已经日趋成熟,但内分泌治疗获得性耐药仍然是临床上面临的巨大挑战。今天本文就乳腺癌内分泌治疗耐药相关信号通路及其最新治疗方案进行了总结,希望给大家带来一些提示和思考~
内分泌药物大盘点
现有内分泌治疗药物主要有5类,包括芳香化酶抑制剂(AI)、促性腺激素释放激素类似物、孕激素类药物、选择性雌激素受体调节剂(SERM)和选择性雌激素受体下调剂(SERD)。
1、选择性ER调节剂
代表药物:他莫昔芬(TAM)、托瑞米芬等
作用机制: 结构类似雌激素,能与雌二醇竞争雌激素受体,与雌激素受体形成稳定的复合物,从而使癌细胞的生长受到抑制。
适用人群: 既适合绝经前也适合绝经后的激素受体阳性的乳腺癌患者。
2、芳香化酶抑制剂
代表药物: 非甾体类(阿那曲唑,来曲唑);甾体类(依西美坦)
作用机制: 绝经后女性卵巢功能衰退,体内雌激素70% 以上是来自肾上腺产生的雄激素前体经芳香化酶作用而生成,芳香化酶抑制剂可以抑制芳香化酶的功能。
适用人群: 适用于绝经后或双侧卵巢已切除的激素受体阳性的乳腺癌,也可以诺雷得合用于绝经前激素受体阳性的乳腺癌患者。
3、促性腺激素释放激素类似物
代表药物: 戈舍瑞林、亮丙瑞林等
作用机制: 通过对垂体持续刺激,抑制垂体分泌促卵泡激素和促黄体激素,从而达到下调雌激素水平的目的。
适用人群: 适用于绝经前激素受体阳性的乳腺癌。
4、选择性ER下调剂
代表药物: 氟维司群
作用机制:可通过与雌激素受体结合,导致受体主要功能基团失活,同时引起雌激素受体降解及信号通路的阻断,引起雌激素、孕激素受体在细胞水平的表达急剧减少,阻止或延缓内分泌治疗的耐药。
适用人群: 适用于他莫昔芬(TAM)或AI治疗失败后绝经后晚期乳腺癌一线标准内分泌治疗药物。
5、性激素类药物
代表药物: 甲地孕酮
作用机制: 孕激素能够对下丘脑促性腺激素释放素进行阻滞,继而减少机体内促卵泡激素、降低促黄体生成素水平,并可诱导肝 α-还原酶提升对机体内雄激素的降解速率,抑制雌激素合成。
适用人群: 可用于晚期乳腺癌的姑息性治疗,并可改善晚期肿瘤患者的食欲和恶病质。
怎么判断自己是否出现了耐药?
内分泌耐药分为原发性耐药和继发性耐药。
① 原发内分泌耐药: 一般指辅助内分泌治疗
不超过2年或者晚期一线内分泌治疗不超过6个月即出现肿瘤复发转移或进展。(原发内分泌耐药可能与ER表观沉默、ER基因突变以及基因多态性有关。)
② 继发内分泌耐药: 一般指辅助内分泌治疗超过2年或者结束后1年内出现复发转移,或者一线内分泌治疗超过6个月出现肿瘤进展。(旁通路的异常激活和编码ERα的基因发生突变是继发内分泌耐药的主要机制之一。)
通常病人是否耐药需要从多方面的数据去判断。
① 主观感受: 患者可能有症状,或者症状加重,这是患者层面最主观的观察,同时也是医生判断的依据之一。
② 客观检查: 比如血液检查,还有一些肿瘤指标是否有升高,肝肾功能,肿瘤部位是否发生变化等等,最准确的就是利用PET-CT检查,可一目了然的了解全身整体状况,达到早期发现病灶和诊断疾病的目的。当然耐药不能只通过一个指标判断,多方面的数据才能得出最后的结论。
其实,通俗的来讲,就是在乳腺癌内分泌治疗过程中没效果了,或者效果越来越差,进展了,就属于耐药了。
为什么会发生耐药?
出现耐药的原因也是比较复杂的,但一般最主要的还是经过药物治疗、癌细胞发展导致的人体一些基因突变等原因。
1、ESR1突变
ESR1突变可能会引起ER活性的提高和ER表达的上调,甚至造成ER信号通路不依赖雌激素水平的持续激活,从而导致患者对AI类药物耐药。在早期乳腺癌中,ESR1基因突变频率不足5%;而晚期乳腺癌患者,尤其是既往接受过AI治疗的患者中,ESR1突变频率增加,约为14%-54%。
2、PI3K/AKT/mTOR通路激活
在ER+乳腺癌中,生长因子受体通路尤其是PI3K/AKT/mTOR通路的活化是内分泌治疗继发耐药的主要机制之一。其中,PI3K整条通路的突变率在乳腺癌中高达70%,包括PIK3CA突变、PI3K其他相关基因的突变或扩增、下游因子如AKT1、AKT2、PDK1等相关基因的突变等。
3、细胞周期检查点改变
细胞周期检查点是细胞周期中的一套保证DNA复制和染色体分配质量的检查机制,是一类负反馈调节机制。当细胞周期进程中出现异常事件,如DNA损伤或DNA复制受阻时,这类调节机制就被激活,及时地中断细胞周期的运行。乳腺癌中细胞周期检查点的改变会导致细胞周期的失调,进而导致内分泌治疗耐药。
4、表观遗传学修饰
表观遗传学修饰是指在DNA序列不发生改变,但在基因表达过程中发生的一组可遗传的变化,包括DNA甲基化、组蛋白修饰和非编码RNA调控。表观遗传学修饰的作用主要是通过改变ER的表达来实现的,ER基因启动子区的甲基化导致ER表达下降,进而参与乳腺癌内分泌治疗的耐药过程。
发生耐药了以后怎么办?
发生耐药了也不用太焦虑,根据耐药原因,都有相应的解救措施。
1、指南推荐
中国抗癌协会乳腺癌诊治指南(2022)中对HR+晚期乳腺癌的解救内分泌治疗的不同情况给予相应的治疗方案:
01:他莫昔芬治疗失败
Ⅰ级推荐:AI+CDK4/6抑制剂(阿贝西利、哌柏西利)(1A);AI+达本胺(1A)。
02:非甾体类AI治疗失败
Ⅰ级推荐:氟维司群+阿贝西利(1A);甾体类AI+西达本胺(1A);氟维司群+达尔西利(2A);氟维司群+哌柏西利(1B)。
03:甾体类AI治疗失败
Ⅰ级推荐:氟维司群+阿贝西利(1A);氟维司群+达尔西利(2A);氟维司群+哌柏西利(1B)。
04:CDK4/6治疗失败
Ⅰ级推荐指南中并没有给出相应治疗方案;在Ⅱ级推荐中,西达本胺+内分泌和另一种CDK4/6抑制剂+内分泌治疗均被作为2A级证据;参加严格设计的临床研究也是Ⅱ级推荐的一种方案。
05:其他Ⅱ、Ⅲ级推荐参考如下指南推荐方案
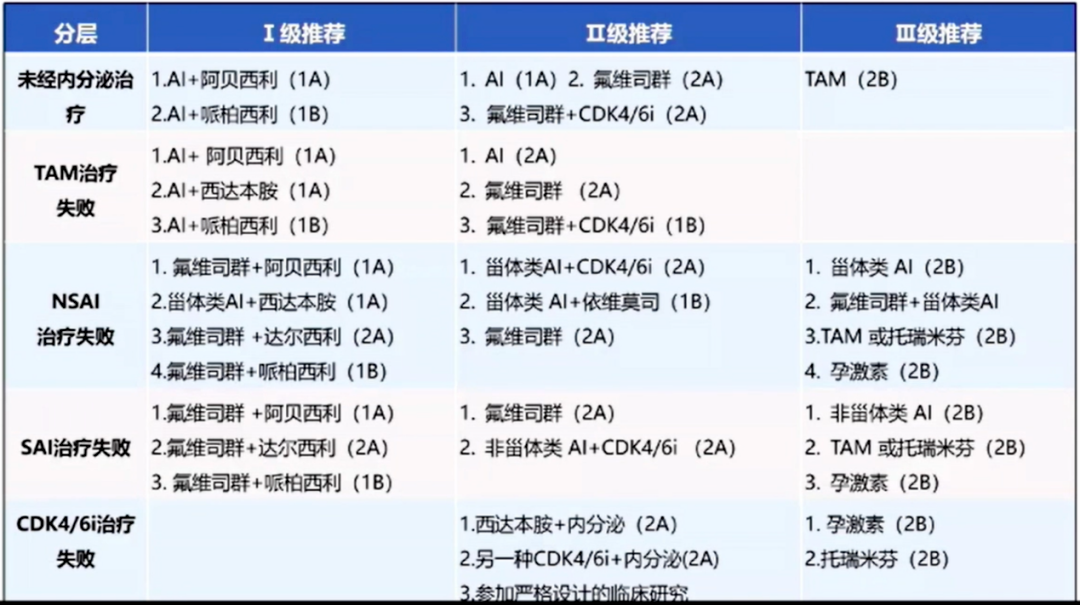
中国抗癌协会乳腺癌诊治指南(2022)推荐内分泌治疗失败后的治疗方案
2、基因检测
无论一线还是后线内分泌治疗耐药的患者,都可行基因检测,取原发灶进展组织、转移灶或外周血样本送检,明确具体耐药原因,进行相应的个体化治疗。
① ESR1基因突变耐药后方案
对AI耐药的患者可改用他莫昔芬、氟维司群、新一代SERM/SERD,以及应用信号通路抑制剂使ER下游转录途径阻断或活性降低等。
其中,新型SERD类药物(如RAD1901、AZD9496、GDC-9545),都在临床试验阶段。关于SERM药物,巴多昔芬已被批准用于骨质疏松症患者,而拉索昔芬是目前在研的一种二代的非甾体SERM。
② PI3K/AKT/MTOR通路相关抑制剂
PI3K/AKT/mTOR 抑制剂包括选择性PI3K抑制剂-阿培利司(Alpelisib)、AKT抑制剂-Capivasertib、mTOR抑制剂-依维莫司(Everolimus)和替西罗莫司(Temsirolimus等)。
其中,FDA已批准阿培利司与氟维司群联合治疗用于内分泌治疗期间或治疗后出现疾病进展的HR+/HER2-,且携带PIK3CA突变的晚期乳腺癌的绝经后女性和男性患者,但目前药物还未在中国上市。
FDA批准依维莫司联合依西美坦用于AI治疗失败的绝经后HR+/HER2-晚期乳腺癌患者的治疗,已在中国上市。
而Capivasertib是首个高选择性口服小分子AKT抑制剂,能够高效地选择性抑制三种AKT亚型(AKT1/2/3)。2019年,FAKTION研究首次在ASCO亮相,Capivasertib+氟维司群联合治疗显著改善了AI耐药后MBC患者的PFS,目前正在开展Ⅲ期临床试验。
综上,内分泌耐药不是世界末日,目前已经有很多种可以使用的解救措施,同时还有很多在研的新药以及开展中的临床试验研究。
参考:若初健康
