1 筛查流程及病例管理流程
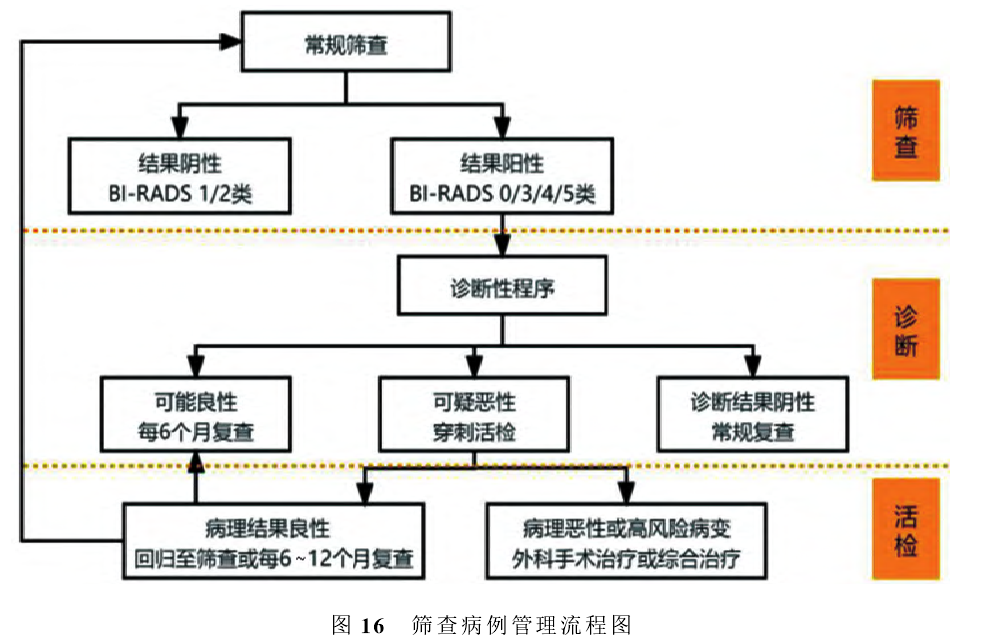
见图15、图16图筛查诊断流程图。

2 数据质控
筛查所需要收集的数据包括原始数据(Raw Da-ta)和衍生数据(Derived Data),原始数据指在乳腺影像检查和病理报告中可以直接获得的信息,衍生数据是利用基础资料数值分别计算。所有数据及指标均需规范化采集并统计,这是保证筛查质量的关键。
为了得到更完整的统计结果,原始数据需补充危险因素、是否为首次检查、乳腺癌的影像学特征、是否可触及等,衍生数据则需补充真阴性和假阴性、筛查中第一年以及随后几年的乳腺癌检出率、不同年龄组的乳腺癌检出率、不可触及性乳腺癌的百分率、不同类别的诊断性检查的异常判读率、灵敏度和特异度等。
评价该影像学检查是否为适宜的筛查方法应符合以下三个基本要求:
第一,通过计算乳腺癌检出率或灵敏度,确定是否在筛查人群中发现了高比例的乳腺癌。
第二,通过计算召回率和阳性预测值,确定召回标准是否合理有效,能够通过适度的进一步影像检查和病理学诊断发现更多的乳腺癌。
第三,通过统计分析,确定是否发现了高比例的体积小、淋巴结阴性、预后好的早期乳腺癌。评估每个筛查机构或影像医师的工作质量最好的方法是与已经发表的标准进行比较,对照年度筛查结果的趋势,有助于分析每个独立机构的筛查结果。
3 召回及随访
(1)召回:①受检者条件限制导致采集图像不满意需召回。②阳性筛查性检查(Positive ScreeningExamination)需召回。阳性筛查性检查是指该检查结果发现异常,需进一步完善诊断性影像检查或病理学诊断。阳性筛查性检查包括BI-RADS 0、3、4和5类病例。
(2)随访:通过电话、家访及医疗机构病案信息调取查阅等方式进行随访,获得每位筛查对象的最终诊断结果与转归信息。
4 乳腺超声报告规范自动乳腺容积超声推荐报告
内容推荐包括患者的基本信息、图像质控评估,并对病变按照BI-RADS词典进行描述,需额外增加冠状面的特征描述,并根据指南给出分类和管理意见。图像质控需在图像判读前完成,报告相关内容仅呈现结论。
4.1 质量控制
①乳腺容积图像位置、深度和分辨率是否合格,腺体是否完整,是否存在干扰诊断的伪像。
②乳头是否呈均匀的低回声,边界清楚,形态规则。
③皮肤是否为连续平滑带状高回声,厚度是否超过2mm。
④皮下组织是否结构清晰。脂肪组织呈低回声,Cooper’s韧带呈条索样高回声,牵拉乳腺小叶穿过脂肪层与皮肤浅层筋膜相连,后方伴声影。
⑤乳房后间隙是否扫查完全,显示清晰。
4.2 报告描述
4.2.1 简要描述腺体构成
(1)均匀腺体型:横切面上高回声腺体层占比大于低回声脂肪层,腺体内无明显的脂肪结构伸入。
(2)均匀脂肪型:横切面上高回声腺体层占比小于低回声脂肪层,腺体内见明显的脂肪结构伸入。
(3)不均质腺体型:横切面上高回声腺体层占比与低回声脂肪层相似,腺体内可见脂肪结构伸入。
4.2.2 描述及对比重要发现
(1)病灶的定位应包括钟点位置、病灶距离皮肤及乳头的距离。不同的容积位置,病灶的位置会有一定误差,选择病灶显示最佳的容积位置 (如中央区病灶,应选择AP位,内侧象限病灶选择MED位,外侧象限病灶选择LAT位)为准。
(2)为了方便 临 床 理 解,重 要 的 发 现 应 该 使 用BI-RADS词 典 标 准 用 词 进 行 描 述, 包 括 病 变 类 型(肿块型或非肿 块 型 病 变)、肿 物 的 形 状、方 位、边缘、回声、后方特征、钙化及伴随征象与特殊病例。
(3)记录冠状面的征象,包括汇聚征、跳跃征、晕环征、白墙征等。
(4)需与之前检查的结果对比,包括体格检查、乳腺X线、MRI等。①初诊患者:已行体格检查、乳房X线检查、MRI或其他影像学检查,乳腺超声应与之关联。如果超声发现为新探及或与其他影像结果无对应关系,应在报告中陈述。②复查患者:原有的病灶需和之前的检查结果做对比,新探及的病灶需记录相关的图像特征。
4.3 报告结论
4.3.1 评估需对超声重要发现给予
BI-RADS分类。在某些情况下,医师可能会给出不完整评估(0类)来要求额外的检查。
(1)评估未完成———0类,需要进一步影像评价和/或与以往影像学检查对比。如局部回声明显不均匀但未发现明确占位、患者乳头溢血但导管内未发现明确占位、复合囊实性肿物无法确定是否存在实性成分或腺体散在强回声点等,均可以提示0类,根据需要选择手持超声、乳腺X线检查和MRI检查。
(2)评估已完成———最终分类
1类:阴性,正常乳腺,无阳性发现。
2类:良性,一个或多个单纯囊肿,乳腺内淋巴结及术后积液,乳腺假体,复杂囊肿,以及随访2~3年以上无变化且无任何超声恶性征象的纤维腺瘤,可分为2类,建议每12个月随访一次。
3类:良性可能性大,恶性风险≤2%。形态规则、边缘完整的纤维腺瘤、复杂性囊肿、簇状微小囊肿、腺病等典型的良性病变和良性病灶的术后改变可以归为3类,建议每6个月随访一次,连续随访24个月病灶无变化,可降为2类,则可每12个月复查一次。
4类:可疑恶性,恶性风险在10%~95%。此类为不具备典型恶性征象但足够怀疑而建议活检,常见的导管内乳头状病变、检查过程中明显增大及缺乏良性特征的病变可归为4类。根据图像恶性程度的不同将其分为4A类(低度怀疑恶性,2%<恶性病灶的可能性≤10%)、4B类(中度怀疑恶性,10%<恶性病灶的可能性≤50%)和4C类(高度怀疑恶性,50%<恶性病灶的可能性<95%。
5类:高度提示恶性,恶性风险≥95%。
6类:已知的活检证实的恶性病灶。这一类是病理证实为恶性肿瘤(穿刺活检后、不完全术后、乳腺癌新辅助化疗期间疗效评估)。
4.3.2 管理每份报告都应包含进一步诊疗建议
应给出明确的建议来指导进一步诊疗,建议包括常规的按年龄筛查、对良性可能的病灶随访观察、经皮或手术活检后患者每年随访以及临床治疗。如果建议影像引导下介入操作,需写明建议引导介入的影像方法,如乳腺 X线照相的立体定位、超声或 MRI的引导。
5 报告示例(工作站自带结构化报告模板)
(1)患者基本信息+图像质控,见图17。

(2)病变描述,见图18。
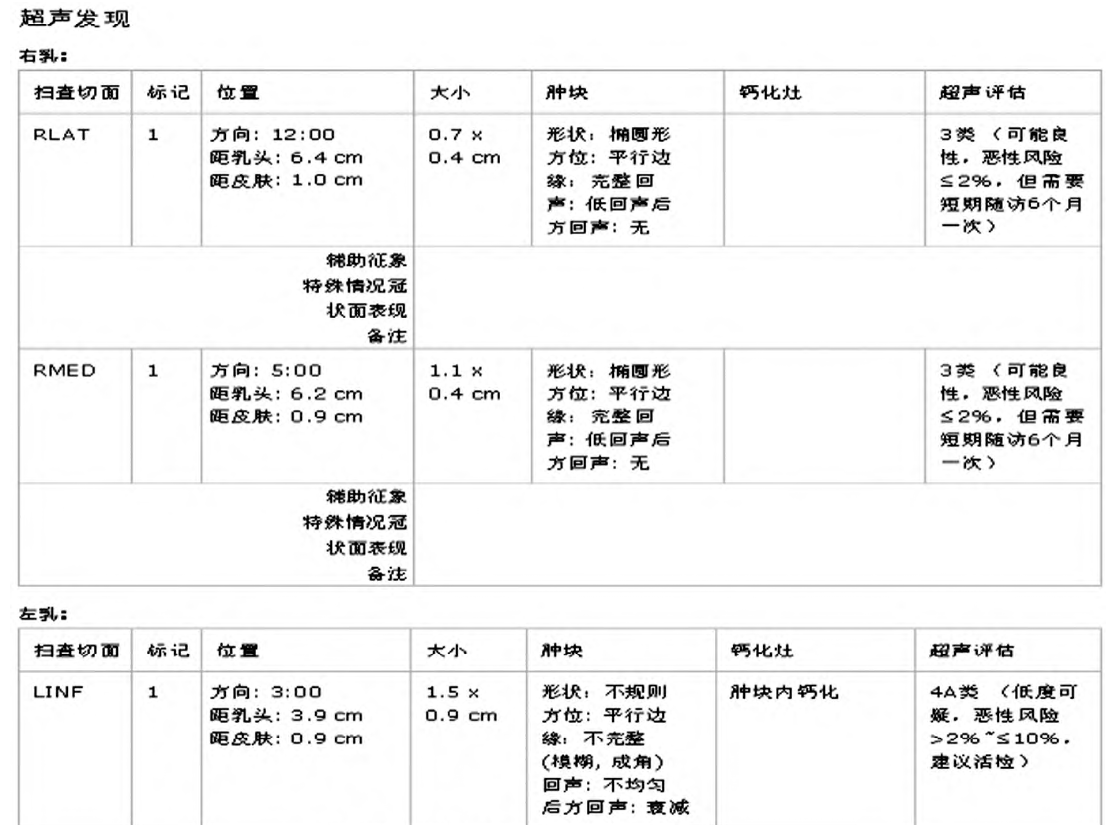

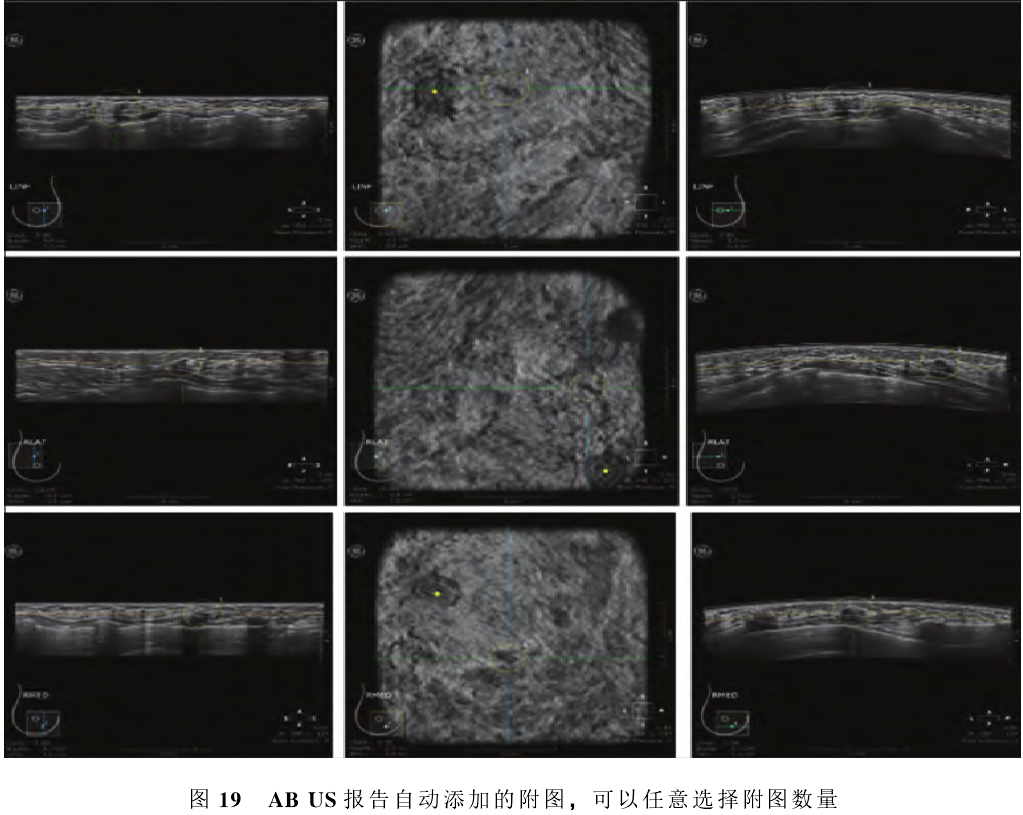
(3)管理建议,见图19。
6 不足与展望
自动乳腺容积超声已成为乳腺癌筛查和诊断的重要辅助手段,并在远程会诊方面展现出较高应用价值和发展前景,但尚存在成像设备大、采集及阅片诊断时间较长等挑战。在用于诊断时由于没有彩色多普勒超声、弹性成像等技术,也无法检查腋窝淋巴结,故无法完全取代手持超声检查。
因此,深度融合人工智能技术与ABUS、大幅提升阅片和诊断效率和精准确度是未来发展的重要方向。李安华与倪东等首次基于深度学习实现兼顾高灵敏度和低假阳率的自动筛查,包凌云等的研究报道了计算机辅助诊断软件可有效提升病灶检出率及阅片和诊断速度。美国FDA批准了Koios Medical公司的病灶辅助检测软件以及Qview Medical公司的QVCAD软件。
ABUS结合人工智能将进一步推动阅片规范化、客观化、智能化,但仍应关注并探究以下问题:①规范流程:智能部署[与PACS(Picture ArchivingAnd Communication System)独立工作,保障数据安全]、智能阅片(无须改变超声设备及工作流程);②全流程智能化:病灶检测、分割、测量、BI-RADS分类、良恶性判别、关键帧选取等;③高效性:提升分析速度及数据传输效率;④结构化报告:一键获取、智能化超声所见及诊断。
未来乳腺癌筛查趋势应以提升早诊率为导向,将筛查服务下沉到基层,助力提升基层筛查的覆盖率和早诊率。上述人工智能技术是提高基层筛查质量不可或缺的重要手段。同时,针对ABUS设备大、采集阅片时间长等挑战,相关技术发展还应面向仪器小型化、提升传输存储效率等方向。随着仪器小型化、5G网络在乡村的铺开、人工智能技术的成熟,乳腺癌筛查走进乡村将成为可能。凭借高效标准化成像、图像快速传回阅片中心和远程会诊,AB US有望成为中国乳腺癌筛查的首选技术,见图20。

参考:自动乳腺容积超声技术专家共识(2022版);中国超声医学工程学会仪器工程开发专业委员会;中国抗癌协会肿瘤影像专委会;中华医学会超声医学分会浅表组织与血管学组(上接38卷第3期)
