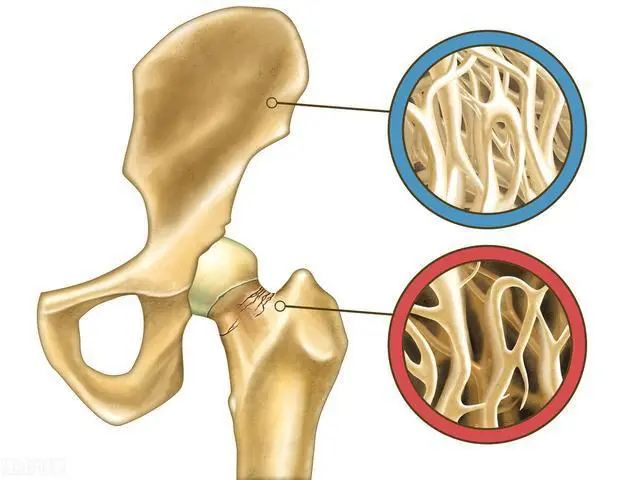
骨质疏松症(OP)是由遗传、环境以及基因-环境相互作用引起的全身性骨病,因骨量减少、骨微结构破坏,导致患者骨脆性增加、易发生骨折。
近年发现,同时患骨质疏松症和恶性肿瘤的人数不断增加,乳腺癌等恶性肿瘤常伴有骨量减少。
研究显示,乳腺癌细胞可以抑制成骨细胞活性,同时导致破骨细胞活性增加,加速溶骨性损伤。
另外,乳腺癌患者体内还可分泌一些细胞因子,使正常的骨代谢发生紊乱,导致OP风险增加,如有些乳腺癌细胞会分泌甲状旁腺激素(PTH)相关蛋白,并作用于PTH受体,促进破骨细胞的作用,引起高钙血症及骨质疏松。
除此之外,乳腺癌的部分治疗措施也可能引起OP。
1 化疗对乳腺癌患者发生OP的影响
化疗后乳腺癌患者的骨矿质含量明显丢失。化疗会对患者的骨骼系统产生明显的不良反应,尤其是长时间的化疗可导致患者出现OP。
化疗药物一般通过三条途径导致性腺机能的损害,致雌激素分泌迅速减少,从而引起OP:
① 通过损伤下丘脑-垂体系统而引起卵巢功能不全;
② 多数抗癌药物可直接作用于卵巢,引起卵巢功能的损害;
③ 化疗药物本身直接导致OP,如大剂量氨甲喋呤通过降低前成骨细胞向成骨细胞增殖和分化,影响骨基质矿化,抑制骨形成并增加骨吸收而使骨量减少。
2 内分泌治疗对乳腺癌患者发生OP的影响
内分泌治疗在改善乳腺癌患者生存率的同时,也显著降低了骨密度(BMD),增加OP和病理性骨折的发生率。
骨是雌激素发挥作用的重要靶器官之一,乳腺癌患者接受内分泌治疗后其体内雌激素水平明显下降,易引起OP。
① 芳香化酶抑制剂(AI)
使机体雌激素下降的速度和程度远远超过了健康的绝经后妇女,对骨质丢失的影响很大,长期应用会导致关节症状(包括关节炎、关节病、关节痛和关节障碍) 及肌肉痛,造成OP和骨折的发生率升高。
② 卵巢功能抑制剂(促黄体激素释放激素类似物)
通过负反馈作用于下丘脑,抑制下丘脑产生促性腺激素释放激素,同时还能抑制垂体产生黄体生成素(LH)和卵泡刺激素(FSH) ,使卵巢分泌雌激素减少。

戈舍瑞林是其代表性药物,它通过抑制卵巢功能而急剧降低循环雌激素水平诱导卵巢萎缩。
3 放疗对乳腺癌患者发生OP的影响
一般认为骨组织对放疗有耐受性,但这只是相对的,如果照射剂量较高或者反复照射,对骨也会有明显损伤。
放疗对骨组织破坏的程度与照射时间和剂量有密切关系,大剂量照射除能直接杀伤骨细胞外,还能间接地引起骨内动脉内腹炎。
4 乳腺癌患者OP的防治
临床根据骨密度(BMD)检测,对患者骨丢失和骨质疏松风险进行评估,应用AI的绝经后乳腺癌患者,当BMD的T值≥-1.0时为低危,-2.0<T值<-1.0为中危,T值≤-2.0或骨折风险评价工具预测10年主要骨折风险>20%或髋骨骨折>3%为高危。
应对所有患者进行生活方式上的干预,建议其每日应进行至少30min中等强度的运动,如步行、慢跑等;进食含钙丰富的食物;戒烟、戒酒;特别注意防止跌倒和身体猛烈撞击。
若依据BMD结果评估为低危者,则应适当补充钙剂和维生素D。此外,应坚持每年进行血25-羟维生素 D及BMD检测并对骨折风险进行评估。中高危患者除需改善生活方式外,还应及时给予适当的药物治疗与管理。乳腺癌患者钙剂、维生素D及双膦酸盐治疗剂量推荐方案见表1。
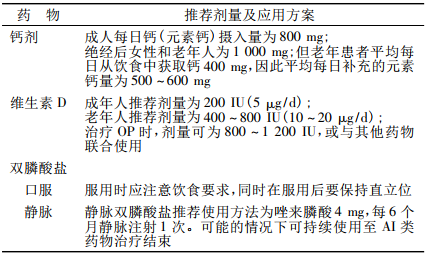
表1 钙剂、维生素D及双膦酸盐的剂量推荐应用方案
注:当钙剂为维生素D与双膦酸盐联合应用时,钙剂为1200~1500mg/d,维生素D为400~800IU/d
药物治疗时建议选择对骨安全性影响较小的药物,以减少骨安全问题的发生。
甾体类AI药物具有独特的雄激素样结构,较非甾体类AI药物对骨安全的影响小,建议高危患者可选择甾体类AI药物治疗。
拒绝接受AI治疗或不能耐受AI类药物的绝经后乳腺癌患者,可服用他莫昔芬,以减少对骨的影响。
雌激素及雌激素受体调节剂会对乳腺癌造成影响,故激素治疗OP比较困难。此类患者应该更加注重钙及维生素D的补充,既能防治OP,也对乳腺癌的骨转移有一定的预防作用。

药物治疗的同时,还应加强骨密度检测频率,建议患者每3~6个月检测1次。
骨质疏松症是慢性疾病,需长期治疗,要达到预期效果,必须预防和治疗相结合,在合理用药的前提下,提高人群及患者对骨质疏松症的认识,养成良好的生活习惯,提高生活质量。
图片来源:网络
参考资料:
戴威,孔令泉,吴凯南.乳腺癌伴随疾病全方位管理之骨健康管理[J].中国临床新医学,2019,12(02):145-149.
